Trastuzumabe no câncer de mama inicial - estudo apt
Trastuzumabe no câncer de mama inicial - estudo apt
Trastuzumabe no câncer de mama inicial - estudo apt
Os tumores de mama HER2-positivos correspondem a cerca de 15 a 20% de todos os tumores de mama. A superexpressão de HER2 está relacionada com tumores mais agressivos, de maior invasividade e potencial metastático. A utilização de trastuzumabe no tratamento dos tumores de mama HER2 não metastáticos modificou a história natural da doença, com redução do risco de recorrência e ganho de sobrevida. Porém a maioria dos estudos se concentrou nos tumores de estádios II e III, e pacientes com tumores menores de 2 cm, sem comprometimento axilar são população minoritária nesses estudos. Embora os tumores HER2-positivos de EC I apresentem menores taxas de recidiva que os mais avançados, a mesma não é desprezível.
O APT é um estudo fase 2, de braço único, que analisou como desfecho primário a sobrevida livre de progressão em pacientes com câncer de mama HEr2 positivo menores que 3 cm, submetidos a quimioterapia com 12 semanas de paclitaxel e 1 ano de trastuzumabe adjuvantes. Foram incluídas 410 pacientes, sendo somente 32,5% com menos de 50 anos, 8,9% com tumores entre 2 e 3 cm, 98,5% sem comprometimento axilar e 67 % dos tumores apresentavam expressão de receptores hormonais.
A taxa de sobrevida livre de doença em 3 anos foi de 98,7% e em uma análise de 7 anos, alcançou 93%, com 4 recorrências (1% da população). Esse benefício em sobrevida livre de doença foi observado na população como um todo, independentemente do status do receptor hormonal( figura 1). A sobrevida global em 7 anos foi de 95%.
Quanto ao subtipo definido pelo PAM50, a maioria dos tumores se classificou como Her2 enriquecido (66%), seguido por luminal B (14%), luminal A ( 13%) e basalóide( 8%), semelhante ao observado em tumores HER2-positivos mais avançados .
Em relação à toxicidade, neuropatia grau 3 ocorreu em 3,2% dos pacientes, 3,2% com queda assintomática da fração de ejeção do ventrículo esquerdo ( 12 de 13 pacientes com reversão da cardiotoxicidade) e 0,5% com sintomas cardíacos congestivos.
Os excelentes resultados observados em sobrevida, firmaram a associação de trastuzumabe com paclitaxel como a opção de tratamento para esses tumores iniciais, favorecendo o tratamento destas pacientes com menor toxicidade em relação aos esquemas de quimioterapia mais agressivos.
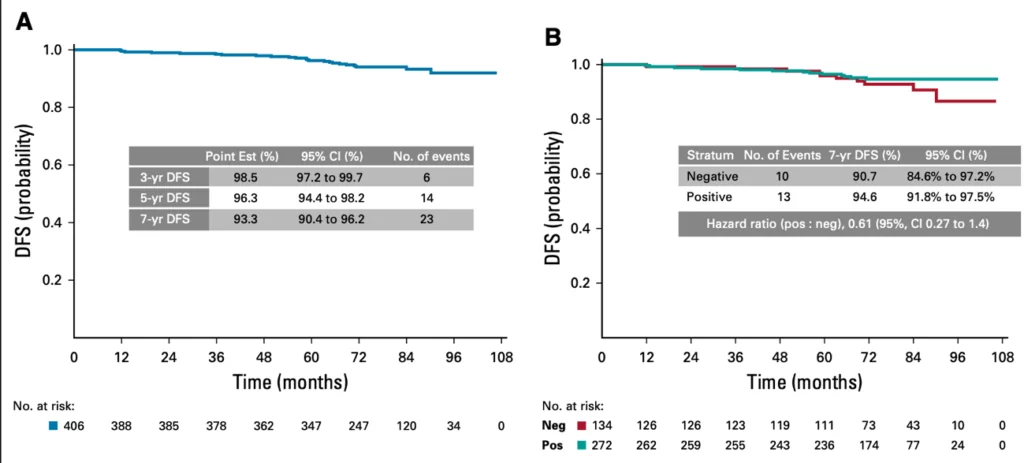
Figura 1: Sobrevida livre de doença da população como um todo (A) e de acordo com receptor hormonal (B)em pacientes com câncer de mama HER2 positivo no estudo APT
Referências
1. Tolaney SM, Barry WT, Dang CT, Yardley DA, Moy B, Marcom PK, Albain KS, Rugo HS, Ellis M, Shapira I, Wolff AC, Carey LA, Overmoyer BA, Partridge AH, Guo H, Hudis CA, Krop IE, Burstein HJ, Winer EP. Adjuvant paclitaxel and trastuzumab for node-negative, HER2-positive breast cancer. N Engl J Med. 2015 Jan 8;372(2):134-41. doi: 10.1056/NEJMoa1406281. Erratum in: N Engl J Med. 2015 Nov 12;373(20):1989. PMID: 25564897; PMCID: PMC4313867. 2. Tolaney SM, Guo H, Pernas S, Barry WT, Dillon DA, Ritterhouse L, Schneider BP, Shen F, Fuhrman K, Baltay M, Dang CT, Yardley DA, Moy B, Marcom PK, Albain KS, Rugo HS, Ellis MJ, Shapira I, Wolff AC, Carey LA, Overmoyer B, Partridge AH, Hudis CA, Krop IE, Burstein HJ, Winer EP. Seven-Year Follow-Up Analysis of Adjuvant Paclitaxel and Trastuzumab Trial for Node-Negative, Human Epidermal Growth Factor Receptor 2-Positive Breast Cancer. J Clin Oncol. 2019 Aug 1;37(22):1868-1875. doi: 10.1200/JCO.19.00066. Epub 2019 Apr 2. PMID: 30939096; PMCID: PMC7587424..

Dra. Solange Sanches
Oncologista Clínica do A.C. Camargo Center
Os tumores de mama HER2-positivos correspondem a cerca de 15 a 20% de todos os tumores de mama. A superexpressão de HER2 está relacionada com tumores mais agressivos, de maior invasividade e potencial metastático. A utilização de trastuzumabe no tratamento dos tumores de mama HER2 não metastáticos modificou a história natural da doença, com redução do risco de recorrência e ganho de sobrevida. Porém a maioria dos estudos se concentrou nos tumores de estádios II e III, e pacientes com tumores menores de 2 cm, sem comprometimento axilar são população minoritária nesses estudos. Embora os tumores HER2-positivos de EC I apresentem menores taxas de recidiva que os mais avançados, a mesma não é desprezível.
O APT é um estudo fase 2, de braço único, que analisou como desfecho primário a sobrevida livre de progressão em pacientes com câncer de mama HEr2 positivo menores que 3 cm, submetidos a quimioterapia com 12 semanas de paclitaxel e 1 ano de trastuzumabe adjuvantes. Foram incluídas 410 pacientes, sendo somente 32,5% com menos de 50 anos, 8,9% com tumores entre 2 e 3 cm, 98,5% sem comprometimento axilar e 67 % dos tumores apresentavam expressão de receptores hormonais.
A taxa de sobrevida livre de doença em 3 anos foi de 98,7% e em uma análise de 7 anos, alcançou 93%, com 4 recorrências (1% da população). Esse benefício em sobrevida livre de doença foi observado na população como um todo, independentemente do status do receptor hormonal( figura 1). A sobrevida global em 7 anos foi de 95%.
Quanto ao subtipo definido pelo PAM50, a maioria dos tumores se classificou como Her2 enriquecido (66%), seguido por luminal B (14%), luminal A ( 13%) e basalóide( 8%), semelhante ao observado em tumores HER2-positivos mais avançados .
Em relação à toxicidade, neuropatia grau 3 ocorreu em 3,2% dos pacientes, 3,2% com queda assintomática da fração de ejeção do ventrículo esquerdo ( 12 de 13 pacientes com reversão da cardiotoxicidade) e 0,5% com sintomas cardíacos congestivos.
Os excelentes resultados observados em sobrevida, firmaram a associação de trastuzumabe com paclitaxel como a opção de tratamento para esses tumores iniciais, favorecendo o tratamento destas pacientes com menor toxicidade em relação aos esquemas de quimioterapia mais agressivos.

Figura 1: Sobrevida livre de doença da população como um todo (A) e de acordo com receptor hormonal (B)em pacientes com câncer de mama HER2 positivo no estudo APT
Referências
1. Tolaney SM, Barry WT, Dang CT, Yardley DA, Moy B, Marcom PK, Albain KS, Rugo HS, Ellis M, Shapira I, Wolff AC, Carey LA, Overmoyer BA, Partridge AH, Guo H, Hudis CA, Krop IE, Burstein HJ, Winer EP. Adjuvant paclitaxel and trastuzumab for node-negative, HER2-positive breast cancer. N Engl J Med. 2015 Jan 8;372(2):134-41. doi: 10.1056/NEJMoa1406281. Erratum in: N Engl J Med. 2015 Nov 12;373(20):1989. PMID: 25564897; PMCID: PMC4313867. 2. Tolaney SM, Guo H, Pernas S, Barry WT, Dillon DA, Ritterhouse L, Schneider BP, Shen F, Fuhrman K, Baltay M, Dang CT, Yardley DA, Moy B, Marcom PK, Albain KS, Rugo HS, Ellis MJ, Shapira I, Wolff AC, Carey LA, Overmoyer B, Partridge AH, Hudis CA, Krop IE, Burstein HJ, Winer EP. Seven-Year Follow-Up Analysis of Adjuvant Paclitaxel and Trastuzumab Trial for Node-Negative, Human Epidermal Growth Factor Receptor 2-Positive Breast Cancer. J Clin Oncol. 2019 Aug 1;37(22):1868-1875. doi: 10.1200/JCO.19.00066. Epub 2019 Apr 2. PMID: 30939096; PMCID: PMC7587424..

Dra. Solange Sanches
Oncologista Clínica do A.C. Camargo Center
Os tumores de mama HER2-positivos correspondem a cerca de 15 a 20% de todos os tumores de mama. A superexpressão de HER2 está relacionada com tumores mais agressivos, de maior invasividade e potencial metastático. A utilização de trastuzumabe no tratamento dos tumores de mama HER2 não metastáticos modificou a história natural da doença, com redução do risco de recorrência e ganho de sobrevida. Porém a maioria dos estudos se concentrou nos tumores de estádios II e III, e pacientes com tumores menores de 2 cm, sem comprometimento axilar são população minoritária nesses estudos. Embora os tumores HER2-positivos de EC I apresentem menores taxas de recidiva que os mais avançados, a mesma não é desprezível.
O APT é um estudo fase 2, de braço único, que analisou como desfecho primário a sobrevida livre de progressão em pacientes com câncer de mama HEr2 positivo menores que 3 cm, submetidos a quimioterapia com 12 semanas de paclitaxel e 1 ano de trastuzumabe adjuvantes. Foram incluídas 410 pacientes, sendo somente 32,5% com menos de 50 anos, 8,9% com tumores entre 2 e 3 cm, 98,5% sem comprometimento axilar e 67 % dos tumores apresentavam expressão de receptores hormonais.
A taxa de sobrevida livre de doença em 3 anos foi de 98,7% e em uma análise de 7 anos, alcançou 93%, com 4 recorrências (1% da população). Esse benefício em sobrevida livre de doença foi observado na população como um todo, independentemente do status do receptor hormonal( figura 1). A sobrevida global em 7 anos foi de 95%.
Quanto ao subtipo definido pelo PAM50, a maioria dos tumores se classificou como Her2 enriquecido (66%), seguido por luminal B (14%), luminal A ( 13%) e basalóide( 8%), semelhante ao observado em tumores HER2-positivos mais avançados .
Em relação à toxicidade, neuropatia grau 3 ocorreu em 3,2% dos pacientes, 3,2% com queda assintomática da fração de ejeção do ventrículo esquerdo ( 12 de 13 pacientes com reversão da cardiotoxicidade) e 0,5% com sintomas cardíacos congestivos.
Os excelentes resultados observados em sobrevida, firmaram a associação de trastuzumabe com paclitaxel como a opção de tratamento para esses tumores iniciais, favorecendo o tratamento destas pacientes com menor toxicidade em relação aos esquemas de quimioterapia mais agressivos.

Figura 1: Sobrevida livre de doença da população como um todo (A) e de acordo com receptor hormonal (B)em pacientes com câncer de mama HER2 positivo no estudo APT
Referências
1. Tolaney SM, Barry WT, Dang CT, Yardley DA, Moy B, Marcom PK, Albain KS, Rugo HS, Ellis M, Shapira I, Wolff AC, Carey LA, Overmoyer BA, Partridge AH, Guo H, Hudis CA, Krop IE, Burstein HJ, Winer EP. Adjuvant paclitaxel and trastuzumab for node-negative, HER2-positive breast cancer. N Engl J Med. 2015 Jan 8;372(2):134-41. doi: 10.1056/NEJMoa1406281. Erratum in: N Engl J Med. 2015 Nov 12;373(20):1989. PMID: 25564897; PMCID: PMC4313867. 2. Tolaney SM, Guo H, Pernas S, Barry WT, Dillon DA, Ritterhouse L, Schneider BP, Shen F, Fuhrman K, Baltay M, Dang CT, Yardley DA, Moy B, Marcom PK, Albain KS, Rugo HS, Ellis MJ, Shapira I, Wolff AC, Carey LA, Overmoyer B, Partridge AH, Hudis CA, Krop IE, Burstein HJ, Winer EP. Seven-Year Follow-Up Analysis of Adjuvant Paclitaxel and Trastuzumab Trial for Node-Negative, Human Epidermal Growth Factor Receptor 2-Positive Breast Cancer. J Clin Oncol. 2019 Aug 1;37(22):1868-1875. doi: 10.1200/JCO.19.00066. Epub 2019 Apr 2. PMID: 30939096; PMCID: PMC7587424..

Dra. Solange Sanches
Oncologista Clínica do A.C. Camargo Center
Os tumores de mama HER2-positivos correspondem a cerca de 15 a 20% de todos os tumores de mama. A superexpressão de HER2 está relacionada com tumores mais agressivos, de maior invasividade e potencial metastático. A utilização de trastuzumabe no tratamento dos tumores de mama HER2 não metastáticos modificou a história natural da doença, com redução do risco de recorrência e ganho de sobrevida. Porém a maioria dos estudos se concentrou nos tumores de estádios II e III, e pacientes com tumores menores de 2 cm, sem comprometimento axilar são população minoritária nesses estudos. Embora os tumores HER2-positivos de EC I apresentem menores taxas de recidiva que os mais avançados, a mesma não é desprezível.
O APT é um estudo fase 2, de braço único, que analisou como desfecho primário a sobrevida livre de progressão em pacientes com câncer de mama HEr2 positivo menores que 3 cm, submetidos a quimioterapia com 12 semanas de paclitaxel e 1 ano de trastuzumabe adjuvantes. Foram incluídas 410 pacientes, sendo somente 32,5% com menos de 50 anos, 8,9% com tumores entre 2 e 3 cm, 98,5% sem comprometimento axilar e 67 % dos tumores apresentavam expressão de receptores hormonais.
A taxa de sobrevida livre de doença em 3 anos foi de 98,7% e em uma análise de 7 anos, alcançou 93%, com 4 recorrências (1% da população). Esse benefício em sobrevida livre de doença foi observado na população como um todo, independentemente do status do receptor hormonal( figura 1). A sobrevida global em 7 anos foi de 95%.
Quanto ao subtipo definido pelo PAM50, a maioria dos tumores se classificou como Her2 enriquecido (66%), seguido por luminal B (14%), luminal A ( 13%) e basalóide( 8%), semelhante ao observado em tumores HER2-positivos mais avançados .
Em relação à toxicidade, neuropatia grau 3 ocorreu em 3,2% dos pacientes, 3,2% com queda assintomática da fração de ejeção do ventrículo esquerdo ( 12 de 13 pacientes com reversão da cardiotoxicidade) e 0,5% com sintomas cardíacos congestivos.
Os excelentes resultados observados em sobrevida, firmaram a associação de trastuzumabe com paclitaxel como a opção de tratamento para esses tumores iniciais, favorecendo o tratamento destas pacientes com menor toxicidade em relação aos esquemas de quimioterapia mais agressivos.

Figura 1: Sobrevida livre de doença da população como um todo (A) e de acordo com receptor hormonal (B)em pacientes com câncer de mama HER2 positivo no estudo APT
Referências
1. Tolaney SM, Barry WT, Dang CT, Yardley DA, Moy B, Marcom PK, Albain KS, Rugo HS, Ellis M, Shapira I, Wolff AC, Carey LA, Overmoyer BA, Partridge AH, Guo H, Hudis CA, Krop IE, Burstein HJ, Winer EP. Adjuvant paclitaxel and trastuzumab for node-negative, HER2-positive breast cancer. N Engl J Med. 2015 Jan 8;372(2):134-41. doi: 10.1056/NEJMoa1406281. Erratum in: N Engl J Med. 2015 Nov 12;373(20):1989. PMID: 25564897; PMCID: PMC4313867. 2. Tolaney SM, Guo H, Pernas S, Barry WT, Dillon DA, Ritterhouse L, Schneider BP, Shen F, Fuhrman K, Baltay M, Dang CT, Yardley DA, Moy B, Marcom PK, Albain KS, Rugo HS, Ellis MJ, Shapira I, Wolff AC, Carey LA, Overmoyer B, Partridge AH, Hudis CA, Krop IE, Burstein HJ, Winer EP. Seven-Year Follow-Up Analysis of Adjuvant Paclitaxel and Trastuzumab Trial for Node-Negative, Human Epidermal Growth Factor Receptor 2-Positive Breast Cancer. J Clin Oncol. 2019 Aug 1;37(22):1868-1875. doi: 10.1200/JCO.19.00066. Epub 2019 Apr 2. PMID: 30939096; PMCID: PMC7587424..

Dra. Solange Sanches
Oncologista Clínica do A.C. Camargo Center
A Bionovis é pioneira na produção e comercialização de medicamentos biológicos e biossimilares.
Nossa busca por inovações científicas e medicamentos de alta complexidade visa construir um Brasil e um mundo mais saudável para todos.
Sobre nós
Relatório de Transparência e Igualdade Salarial de Mulheres e Homens
Institucional
+55 19 3881 5000

SAC
0800 388 5000
LGPD
© 2024 Bionovis. Companhia Brasileira de Biotecnologia Farmacêutica.
A Bionovis é pioneira na produção e comercialização de medicamentos biológicos e biossimilares.
Nossa busca por inovações científicas e medicamentos de alta complexidade visa construir um Brasil e um mundo mais saudável para todos.
Sobre nós
Relatório de Transparência e Igualdade Salarial de Mulheres e Homens
Institucional
+55 19 3881 5000

SAC
0800 388 5000
LGPD
© 2024 Bionovis. Companhia Brasileira de Biotecnologia Farmacêutica.
A Bionovis é pioneira na produção e comercialização de medicamentos biológicos e biossimilares.
Nossa busca por inovações científicas e medicamentos de alta complexidade visa construir um Brasil e um mundo mais saudável para todos.
Sobre nós
Relatório de Transparência e Igualdade Salarial de Mulheres e Homens
Institucional
+55 19 3881 5000

SAC
0800 388 5000
LGPD
© 2024 Bionovis. Companhia Brasileira de Biotecnologia Farmacêutica.
A Bionovis é pioneira na produção e comercialização de medicamentos biológicos e biossimilares.
Nossa busca por inovações científicas e medicamentos de alta complexidade visa construir um Brasil e um mundo mais saudável para todos.
Sobre nós
Relatório de Transparência e Igualdade Salarial de Mulheres e Homens
Institucional
+55 19 3881 5000

SAC
0800 388 5000
LGPD
© 2024 Bionovis. Companhia Brasileira de Biotecnologia Farmacêutica.

